中國干細胞新藥研發(fā)正在以全新的速度前進,?已有近103項干細胞藥物臨床試驗申請獲得受理,?其中多款干細胞新藥已進入臨床研究階段?。?
近年來,?在政策推動下,?我國干細胞產(chǎn)業(yè)迅速擴張,?干細胞新藥研發(fā)速度明顯加快。?據(jù)統(tǒng)計,?截至2024年09月2號,?國內(nèi)共有103項干細胞藥物臨床試驗申請獲得受理。
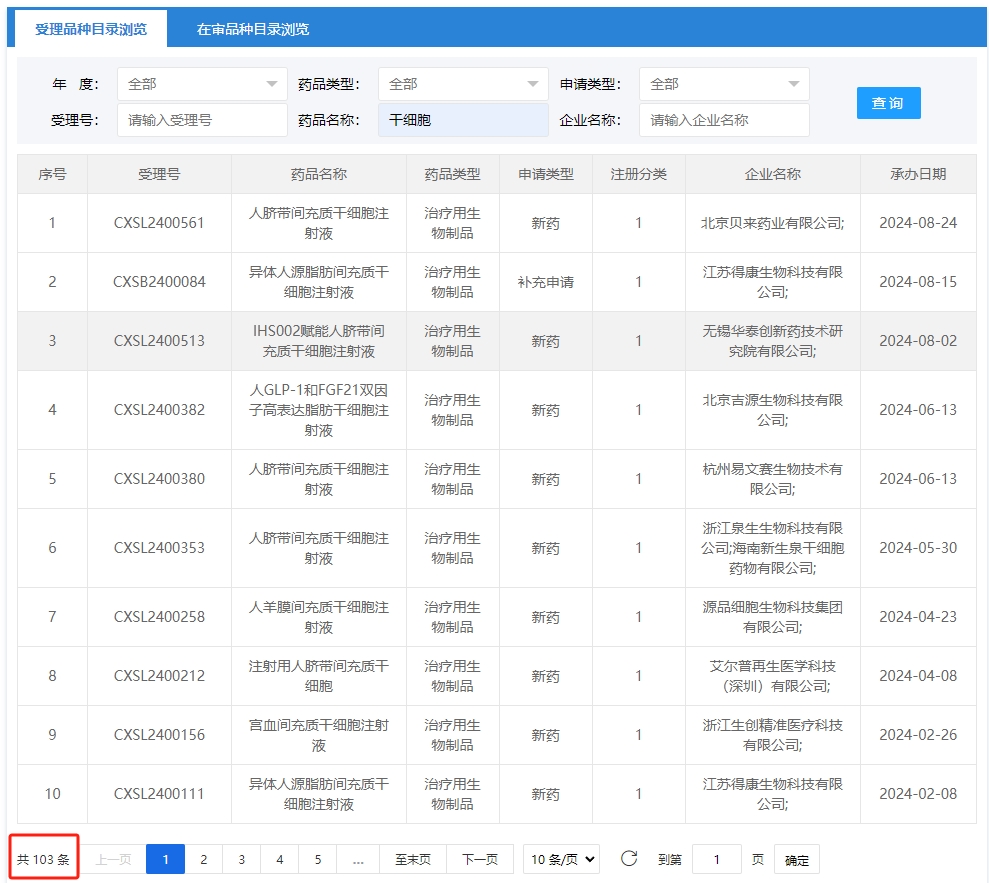
其中截至到2024年1月1號到9月2號新增申報獲受理數(shù)量達到12項。
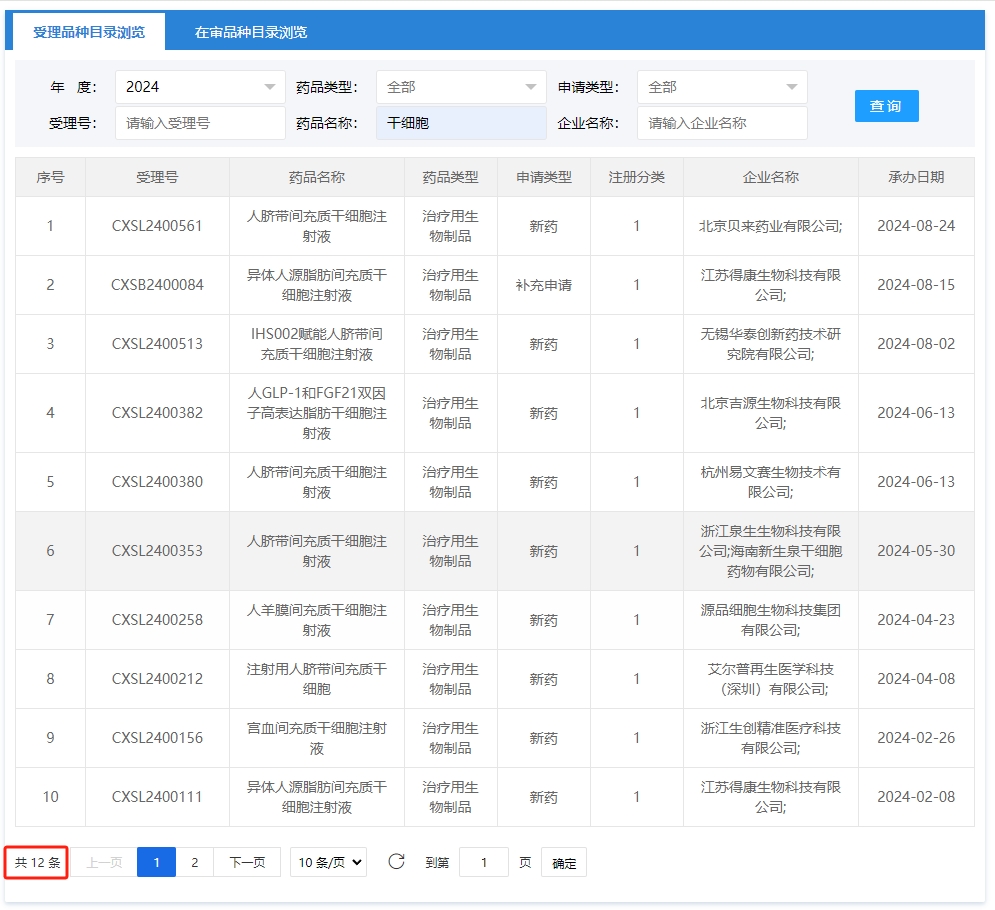
其中,截至2024年9月1號共有54家企業(yè)(不含子公司)的110款獲準默許進入臨床試驗(臨床試驗默示許可)。
這些干細胞新藥涵蓋了多種類型,?如間充質(zhì)干細胞、?造血干細胞、?神經(jīng)干細胞等,?并廣泛應用于治療神經(jīng)系統(tǒng)疾病、?心腦血管疾病、?血液系統(tǒng)疾病等。?目前,?已有多個干細胞藥物進入臨床Ⅲ期,?預示著中國干細胞新藥研發(fā)即將迎來爆發(fā)式增長。
截至2024年9月2號,干細胞新藥受理新增12項
12項干細胞新藥受理的公司是哪些,受理的干細胞新藥適應癥主要是哪些?
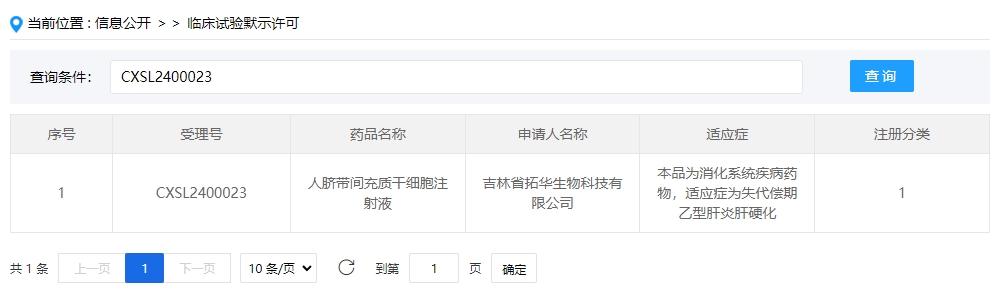
2024年干細胞新藥受理第1項:2024年01月10號,吉林省拓華生物科技有限公司的“人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400023)。
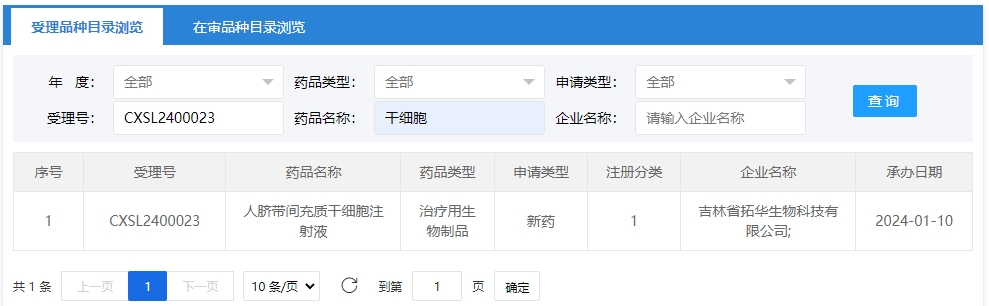
該干細胞新藥的適應癥為消化系統(tǒng)疾病藥物,適應癥為失代償期乙型肝炎肝硬化。
這是該款細胞注射液的第2種適應癥獲得受理,早在2023年02月23日,蘇州拓華生物科技有限公司的“人臍帶間充質(zhì)干細胞注射液”已獲得默示許可(受理號:CXSL2300152)。該干細胞新藥的適應癥為中/重度急性呼吸窘迫綜合癥。
2024年干細胞新藥受理第2項:2024年02月10號,深圳市北科生物科技有限公司的“人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400092)。
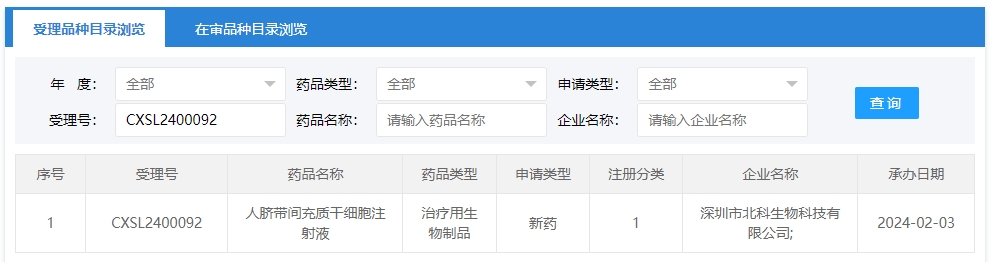
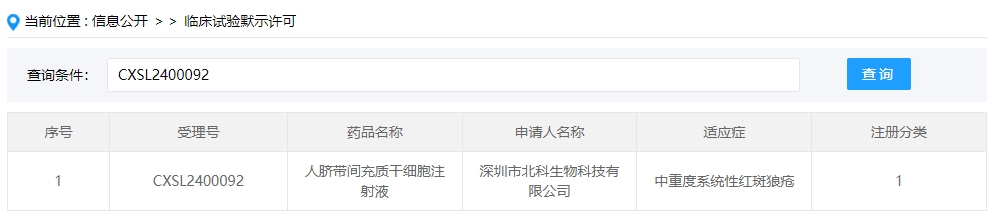
該干細胞新藥的適應癥為中重度系統(tǒng)性紅斑狼瘡。此前,該款干細胞制劑于2020年6月5日獲得受理(受理號:CXSL2000128),但后續(xù)任務進展無法查詢。
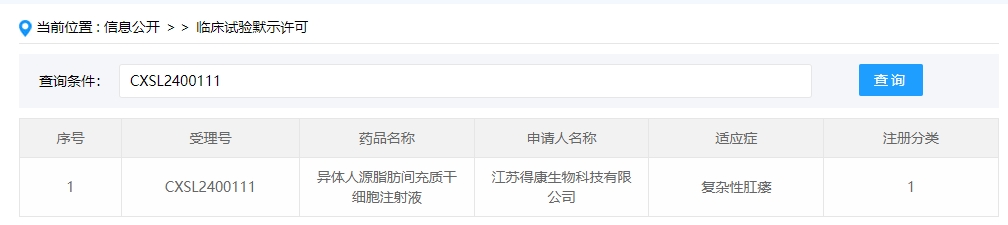
2024年干細胞新藥受理第3項:2024年02月08號,江蘇得康生物科技有限公司的“異體人源脂肪間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400111)。
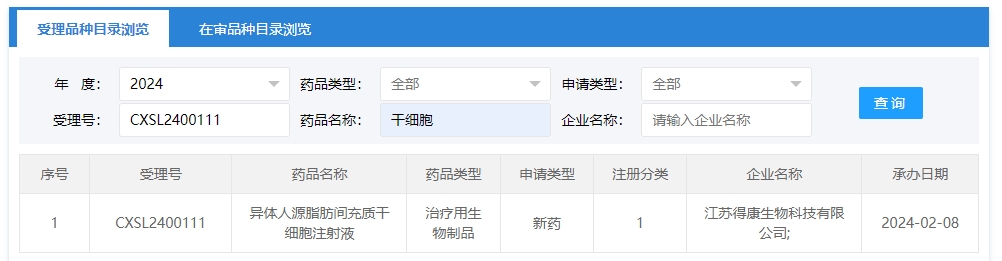
該干細胞新藥的適應癥為復雜性肛瘺。
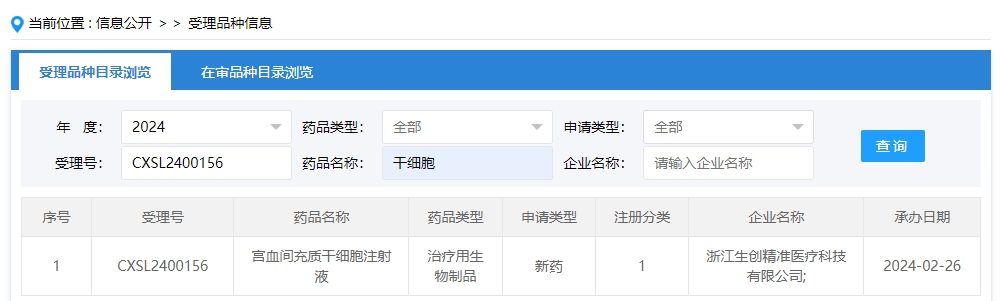
2024年干細胞新藥受理第4項:2024年02月26號,浙江生創(chuàng)精準醫(yī)療科技有限公司的“宮血間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400156)。
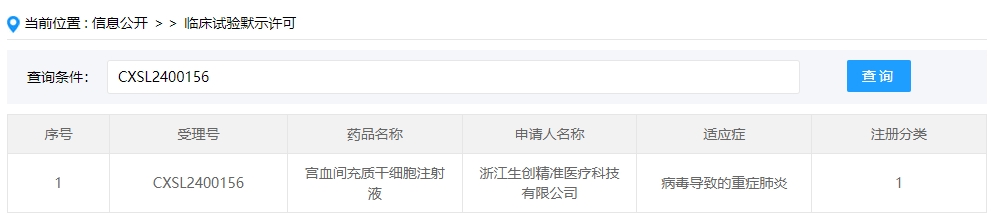
該企業(yè)的干細胞新藥的適應癥為病毒導致的重癥肺炎。
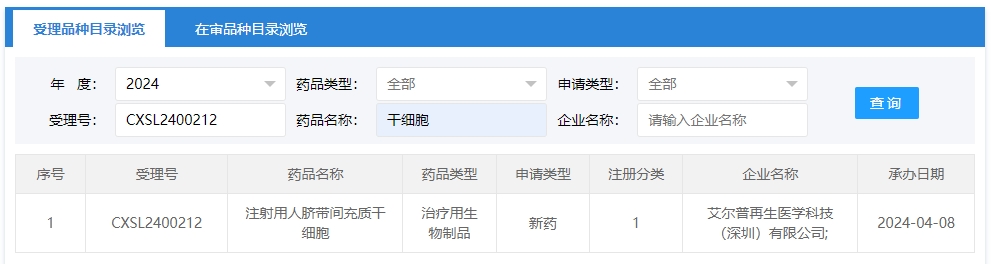
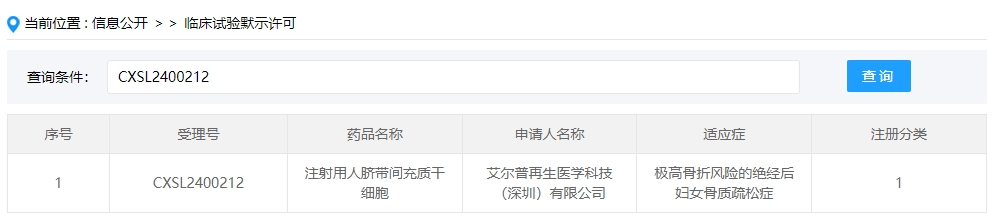
2024年干細胞新藥受理第5項:2024年04月08號,艾爾普再生醫(yī)學科技(深圳)有限公司的“注射用人臍帶間充質(zhì)干細胞”的臨床試驗申請獲受理(受理號為:CXSL2400212)。
該企業(yè)的干細胞新藥的適應癥為極高骨折風險的絕經(jīng)后婦女骨質(zhì)疏松癥。
2024年干細胞新藥受理第6項:2024年04月23號,源品細胞生物科技集團有限公司的“人羊膜間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400258)。
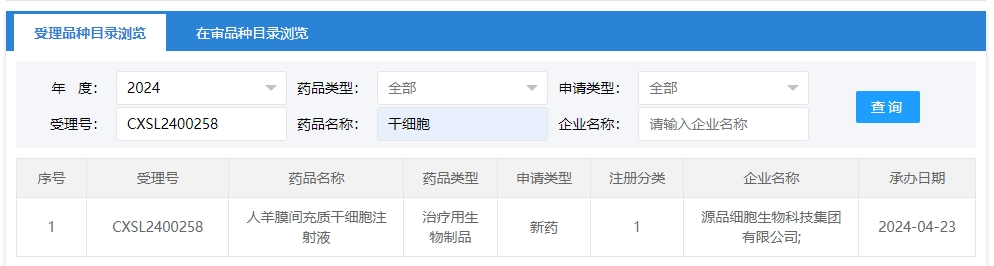
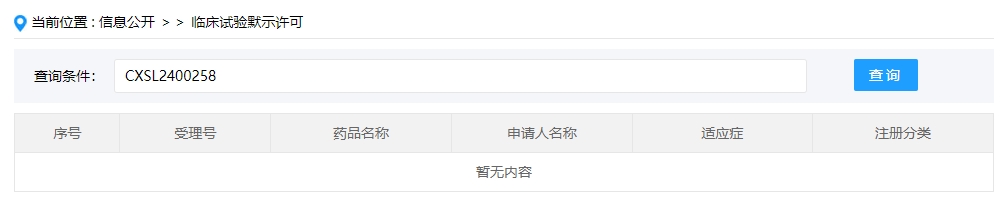
該企業(yè)的干細胞新藥的適應癥暫未查詢到。
2024年干細胞新藥受理第7項:2024年05月30號,浙江泉生生物科技有限公司;海南新生泉干細胞藥物有限公司的“人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400353)。這是該款細胞注射液第6次獲得受理。
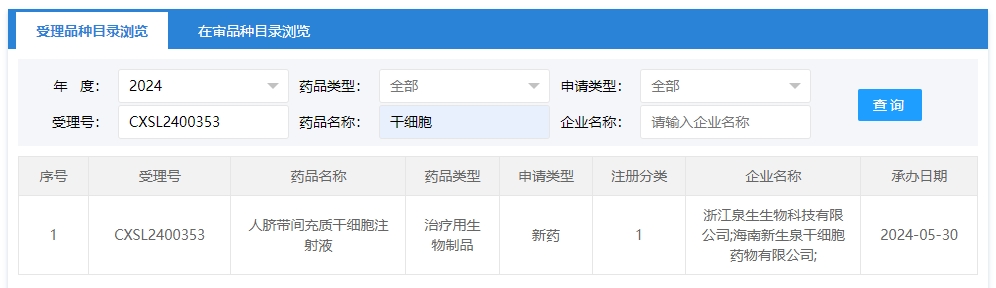
該企業(yè)受理的干細胞新藥適應癥為:此前已默示許可開展注射給藥用于輕至中度急性呼吸窘迫綜合征(ARDS)患者的治療(受理號:CXSL2200114)、注射給藥用于強直性脊柱炎(受理號:CXSL2200299)、注射給藥用于Ⅱ度燒傷(受理號:CXSL2200301)、注射給藥用于失代償期乙肝病毒肝硬化(受理號:CXSL2200457)、注射給藥用于慢性阻塞性肺疾病(受理號:CXSL2300795)的臨床試驗。
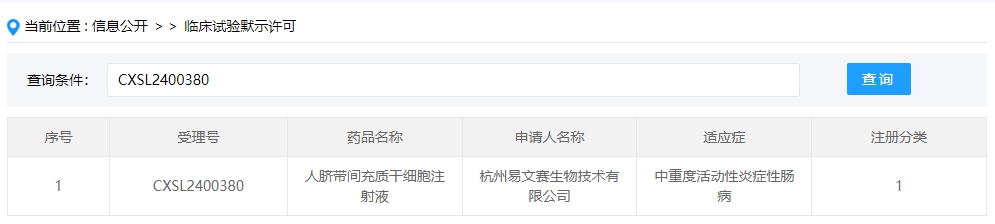
2024年干細胞新藥受理第8項:2024年06月13號,杭州易文賽生物技術(shù)有限公司;的“人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400380)獲得受理。
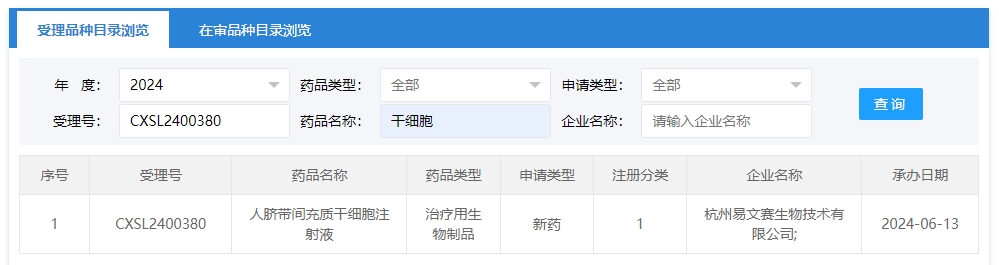
該企業(yè)的干細胞新藥的適應癥為中重度活動性炎癥性腸病。
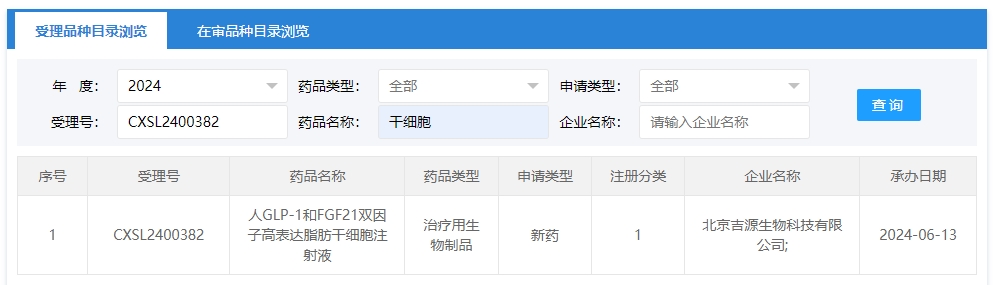
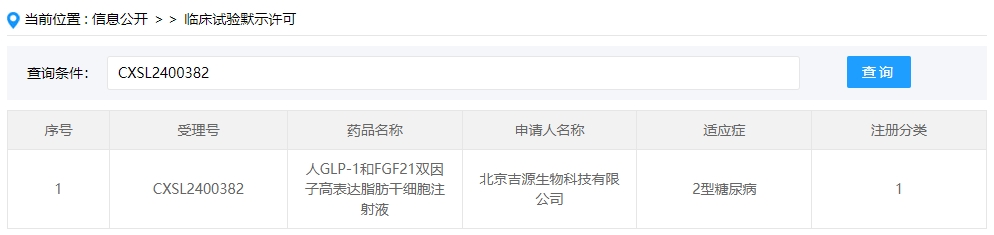
2024年干細胞新藥受理第9項:2024年06月13號,北京吉源生物科技有限公司的“人GLP-1和FGF21雙因子高表達脂肪干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400382)獲得受理。
2024年干細胞新藥受理第10項:2024年08月02號,無錫華泰創(chuàng)新藥技術(shù)研究院有限公司的“IHS002賦能人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400513)獲得受理。
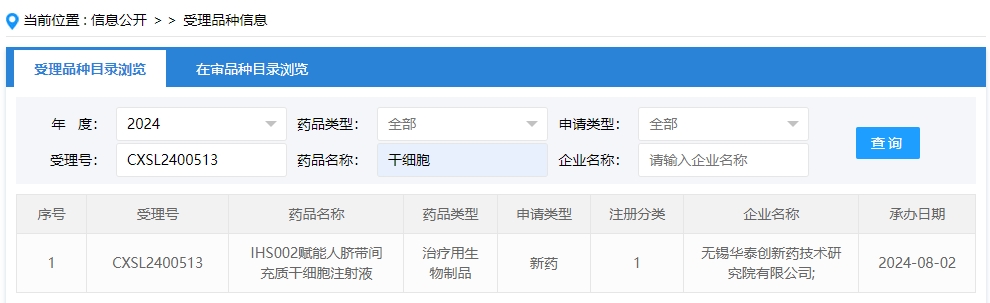
該企業(yè)的干細胞新藥的適應癥暫未查詢到。
2024年干細胞新藥受理第11項:2024年08月15號,江蘇得康生物科技有限公司的“異體人源脂肪間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSB2400084)獲得受理。
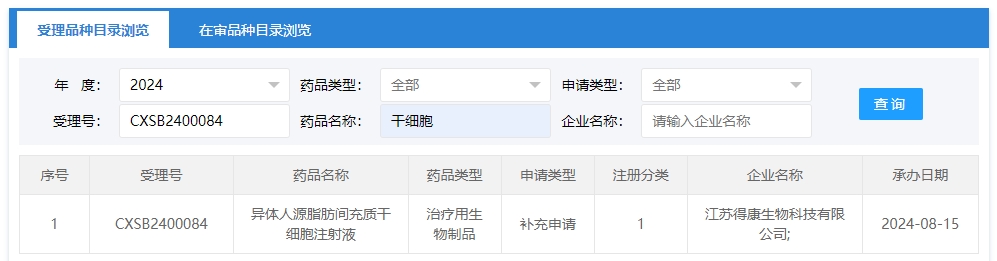
該企業(yè)的干細胞新藥的適應癥暫未查詢到。
2024年干細胞新藥受理第12項:2024年08月24號,北京貝來藥業(yè)有限公司的“異體人臍帶間充質(zhì)干細胞注射液”的臨床試驗申請獲受理(受理號為:CXSL2400561)獲得受理。這是該款細胞注射液第5次獲得受理。
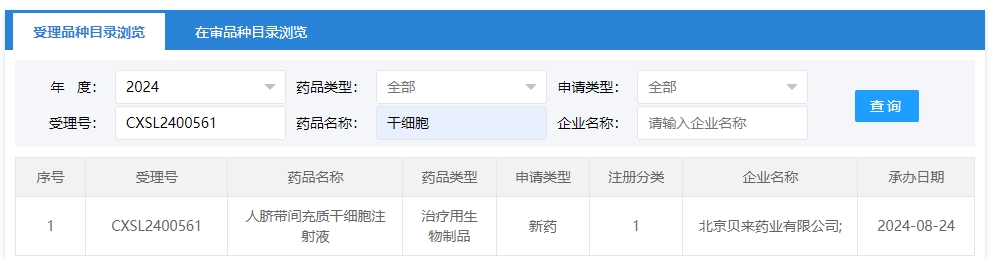
該企業(yè)受理的干細胞新藥適應癥為:這是該款干細胞注射液的第5種適應癥獲得受理,(受理號為:CXSL2400561,適應癥未知),(受理號為:CXSL2300776,適應癥未知),類風濕關(guān)節(jié)炎(CXSL2000005),特發(fā)性肺纖維化(CXSL2200370),阿爾茨海默病(CXSL2300129)。
展望未來
全球細胞治療領域在基礎研究領域已取得諸多重大原創(chuàng)性成果,我國名列前茅。
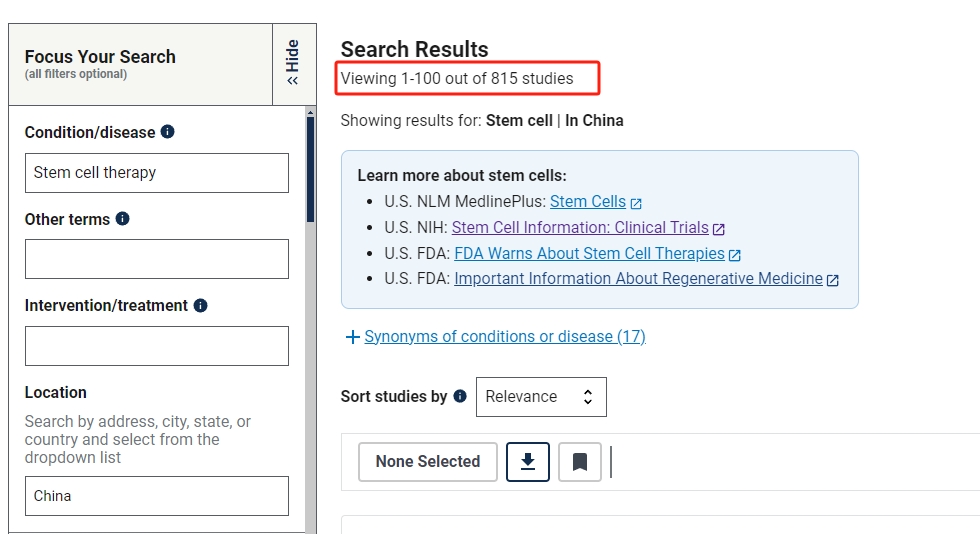
截止2024年9月,在美國國立衛(wèi)生研究院的最大臨床試驗注冊庫clinicaltrials.gov網(wǎng)站上注冊的有關(guān)干細胞治療的臨床研究項目有2693項。
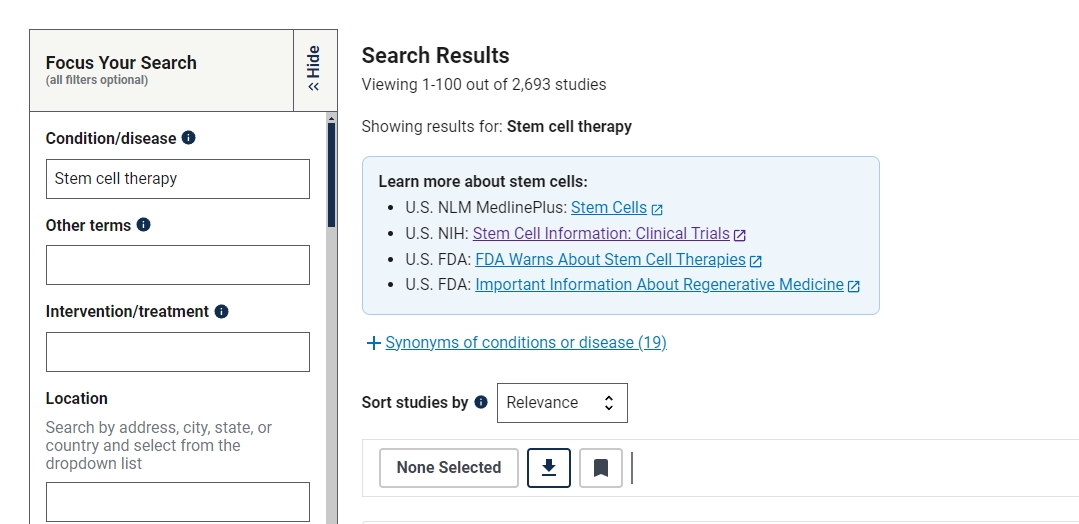
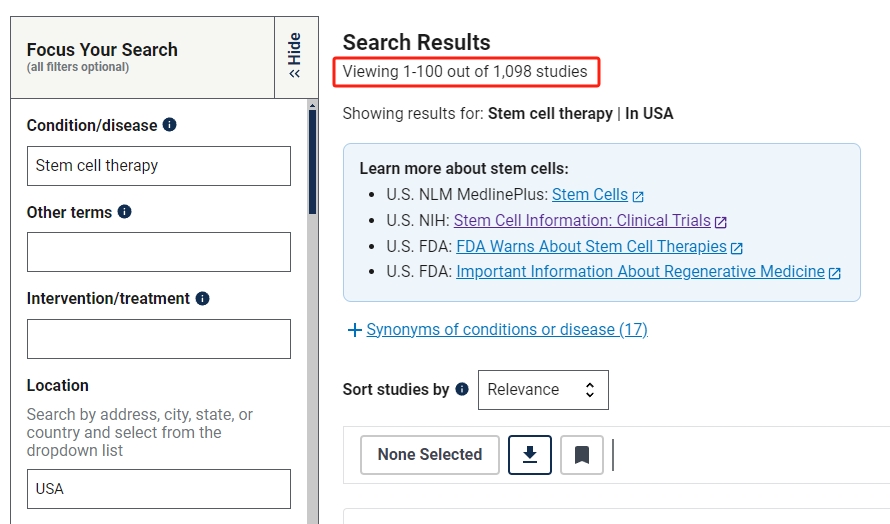
其中在中國進行的干細胞臨床研究的項目有815項,美國為1098項,中美兩國在干細胞工程技術(shù)與基因工程技術(shù)并駕齊驅(qū)。
相信2024年度會是干細胞藥物研發(fā)的爆發(fā)期,會有更多針對新適應癥的細胞藥物進入臨床試驗階段。同時,正在開展干細胞藥物Ⅰ期/Ⅱ期臨床試驗也將逐步產(chǎn)生結(jié)果,相信隨著干細胞技術(shù)研發(fā)的不斷深入,干細胞作為治療藥物離上市將在不遠的未來。
免責說明:本文僅用于傳播科普知識,分享行業(yè)觀點,不構(gòu)成任何臨床診斷建議!杭吉干細胞所發(fā)布的信息不能替代醫(yī)生或藥劑師的專業(yè)建議。如有版權(quán)等疑問,請隨時聯(lián)系我。




 掃碼添加官方微信
掃碼添加官方微信