近年來,干細胞療法為脊髓損傷(SCI)的治療提供了新的研究方向。
干細胞治療脊髓損傷:Ⅰ期臨床試驗1例報告 | 安全性與初步療效
Mohamad等人近期在《MAYO CLINIC PROCEEDINGS》發表了一項利用脂肪組織來源的間充質干細胞(AD-MSCs)治療1例脊髓損傷患者的Ⅰ期臨床試驗。該個案顯示,患者在多項功能指標上出現顯著改善,初步支持該療法在安全性和神經功能恢復方面的潛力。

脊髓損傷是一種嚴重的中樞神經系統損傷,常導致不可逆的神經功能喪失及多系統并發癥,其病理機制涉及原發損傷后的缺血、炎癥反應及繼發性細胞死亡。
患者資料:一名53歲男性,因沖浪事故導致C3-4 SCI,神經系統檢查顯示,損傷水平以下的運動和感覺功能完全喪失,同時腸道和膀胱感覺喪失,被診斷為(ASIA)A級SCI,后接受了C2-6頸后路減壓和融合術,入組時他的神經系統狀態為C級。
治療方法上,研究人員在患者受傷9個月后采集其腹壁脂肪組織,從中分離并擴增AD-MSCs,隨后通過腰椎穿刺于L3-4水平鞘內注射1億個懸浮于乳酸林格氏液中的AD-MSCs。

結果:①亞洲運動評分:上肢運動總分從基線的35分,提高到18個月的44分,與左側相比,右側的改善更為明顯(圖1A和表1);下肢運動總分從基線的36分到18個月的49分(圖1A和表1)。

②亞洲感官評分:總針刺評分從基線的45分提高到18個月的95分,右側從基線的25分改善到18個月的46分,左側從基線的20分改善到18個月的49分;輕觸總分也從基線的54分提高到18個月的96分,右側從基線的27分升至18個月的46分,左側從基線的27分升至18個月的50分(圖1B和表1)。

我們還觀察了患者每個皮節區域的改善情況,發現上肢雙側C5區域的改善非常明顯,左側的C2-4、C6和T1-3區域也有明顯改善;下肢的L4、L5和S1-4區域也得到改善(圖2A和B;3A-D)。

③上肢能力評分:從基線的110分提高到18個月的144分。最顯著的進步是“用手臂拉和推”部分,從基線的31分提高到18個月的46分,以及“使用手和手指”部分,從基線的40分提高到18個月的51分(圖1C)。
④健康得分:全球身體健康原始/T評分,從基線時的8/29.6提高到18個月的10/34.9;全球心理健康評分也從基線的7/11提高到18個月的11/41.1。
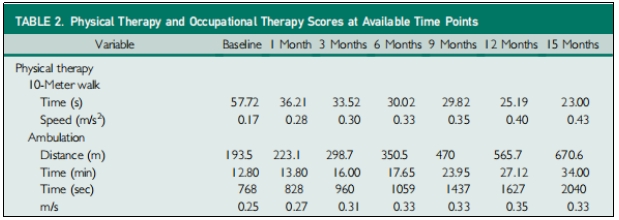
⑤行走能力:患者10米步行測試的時間和速度,從基線的57.72秒(0.17 m/s)提高到15個月的23.00秒(0.43 m/s);行走能力也從基線0.25 m/s的速度行走635英尺,提高到15個月0.33 m/s的速度行走2200英尺(表2)。
⑥安全性和不良事件:患者對手術的耐受性良好,沒有出現任何與注射相關的嚴重不良事件,僅在輸注第2天出現輕度至中度頭痛,使用對乙酰氨基酚后緩解。在18個月的隨訪中,沒有報告其它安全問題或不良事件。
該案例首次報道了鞘內注射脂肪間充質干細胞治療脊髓損傷的初步積極結果,顯示其在運動、感覺、生活質量和行走能力等多方面可能帶來獲益。盡管結果令人鼓舞,鑒于此為單例報告,其療效和安全性仍需通過更大樣本的隨機對照試驗進一步驗證。
參考資料:
Mohamad Bydon, MD; Allan B. Dietz, PhD; Sandy Goncalves, MS;F M Moinuddin, PhD; Mohammed Ali Alvi, MBBS; Anshit Goyal, MBBS;Yagiz Yolcu, MD; Christine L. Hunt, DO; Kristin L. Garlanger, DO;Anna S. Del Fabro, MD; Ronald K. Reeves, MD; Andre Terzic, MD, PhD;Anthony J. Windebank, MD; and Wenchun Qu, MD, PhD, MS. CELLTOP Clinical Trial: First Report From a Phase 1 Trial of Autologous Adipose TissueeDerived Mesenchymal Stem Cells in the Treatment of Paralysis Due to TraumaticSpinal Cord Injury. https://doi.org/10.1016/j.mayocp.2019.10.008.
免責說明:本文僅用于傳播科普知識,分享行業觀點,不構成任何臨床診斷建議!杭吉干細胞所發布的信息不能替代醫生或藥劑師的專業建議。如有版權等疑問,請隨時聯系我。




 掃碼添加官方微信
掃碼添加官方微信